Chemisch element Inhoud Atoomsoort Nieuwe elementen Symbool Enkelvoudige stof Zie ook NavigatiemenuChemisch element
Chemisch element
AtoomBindingElementEnergieEvenwichtFaseIonReactieRedoxMolecuulVerbindingAnalytische chemieAnorganische chemieFysische chemieIndustrieKernchemieOrganische chemieTheoretische chemieprotonenatoomkernatoomnummerperiodiek systeem der elementenkoolstofuranium (uraan)Dmitri MendelejevneutronenisotopenmassagetalsynthetischInternational Union of Pure and Applied Chemistryununseptiumnihoniummoscoviumtennessineoganessonhogere elementenenkelvoudige stofniet-ontleedbare stofzuivere stof
Chemisch element
Naar navigatie springen
Naar zoeken springen
Deel van een serie artikelen over Scheikunde |
 |
|---|
Instrumenten voor analytische chemie |
| ––– Algemeen ––– |
Atoom · Binding · Element · Energie · Evenwicht · Fase · Ion · Reactie · Redox · Molecuul · Verbinding |
| ––– Hoofdtoepassingen ––– |
Analytische chemie · Anorganische chemie · Fysische chemie · Industrie · Kernchemie · Organische chemie · Theoretische chemie |
Portaal |
Chemisch element (vaak kortweg element) heeft twee betekenissen:[1]
- Atoomsoort
- Enkelvoudige stof
Inhoud
1 Atoomsoort
2 Nieuwe elementen
3 Symbool
4 Enkelvoudige stof
5 Zie ook
Atoomsoort
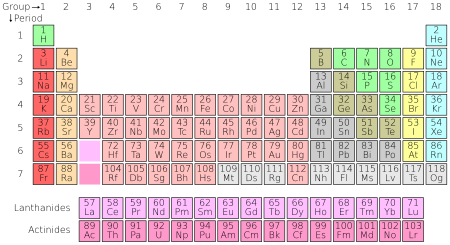
Chemisch element in de betekenis van atoomsoort: alle atomen met hetzelfde aantal protonen in de atoomkern, dus met hetzelfde atoomnummer Z. Het getal Z bepaalt de plaats van het element in het periodiek systeem der elementen, vaak kortweg het periodiek systeem genoemd.
Zo bezitten bijvoorbeeld alle atomen die tot het element koolstof behoren 6 protonen in de kern, en behoren alle atomen met 92 protonen in de kern tot het element uranium (uraan).
Het periodiek systeem werd in 1869 door de Rus Dmitri Mendelejev bedacht, toen nog veel elementen niet ontdekt of slecht onderzocht waren. Vanaf toen maakte het periodiek systeem het mogelijk om van deze nog onbekende elementen veel eigenschappen te voorspellen.
In het periodiek systeem zijn de elementen naar oplopend atoomnummer Z geordend en onderverdeeld in groepen met overeenkomstige eigenschappen en perioden. Atomen die tot eenzelfde element behoren kunnen wel een verschillend aantal neutronen hebben. Men spreekt dan van isotopen. De naam isotoop komt van het Griekse iso = gelijk en topos = plaats, hiermee wordt bedoeld dat isotopen dezelfde plaats in het periodiek systeem innemen. Isotopen van eenzelfde element hebben een verschillend aantal neutronen in de kern en daardoor een verschillend massagetal. De chemische eigenschappen van een element worden vrijwel geheel bepaald door het aantal protonen in de atoomkern. Atomen die tot eenzelfde element behoren kunnen ook een verschillend aantal elektronen bevatten. Een atoom waarbij het aantal elektronen afwijkt van het per element vaste aantal protonen wordt een ion genoemd. Ionen bezitten dus altijd een bepaalde elektrische lading; positief als het aantal elektronen kleiner is dan het aantal protonen, of negatief als het aantal elektronen groter is dan het aantal protonen.
Nieuwe elementen
Men denkt dat alle in de natuur voorkomende stabiele atomen inmiddels bekend zijn. Elementen met atoomnummers hoger dan 92 (uranium) zijn in de natuur niet gevonden, maar wel synthetisch gemaakt. Wanneer een nieuw element voor het eerst kunstmatig gecreëerd wordt, dient dit element een officiële naam te krijgen. Er is een internationale organisatie, de International Union of Pure and Applied Chemistry (IUPAC) (Nederlands: Internationale Unie voor Zuivere en Toegepaste Chemie), die hierover beslist. Deze instantie neemt meestal de naam over die de ontdekker voorgesteld heeft. Soms leidt dit tot controverses, omdat meerdere personen of groepen de ontdekking of synthese voor zich opeisen. Om deze reden heeft het lang geduurd voordat de elementen met een atoomnummer van 104 of hoger een naam kregen.
Tot eind 2016 hadden hogere elementen nog geen echte naam, maar werden ze aangeduid met namen als ununseptium, wat kan worden vertaald als honderdzeventienium, verwijzend naar hun atoomnummer. Met de definitieve benoeming van nihonium, moscovium, tennessine en oganesson door de IUPAC op 28 november 2016 hebben alle elementen in het periodiek systeem een naam gekregen.
Symbool
Elk element krijgt een uniek symbool, dat meestal uit twee letters bestaat, soms één of drie. De eerste letter is altijd een hoofdletter, de andere nooit, zodat er geen verwarring mogelijk is als een aantal symbolen achter elkaar worden geschreven. De elementen die in de scheikunde veel voorkomen, hebben meestal een symbool van één letter. De belangrijkste daarvan zijn waterstof (H), koolstof (C), stikstof (N) en zuurstof (O). De hogere elementen waarvan de voorlopige naam begint met un- hebben een symbool van drie letters.
Het symbool is vaak een afkorting van de Latijnse benaming. De elementen die al lange tijd bekend zijn hebben in verschillende talen uiteenlopende namen. Het internationale symbool voorkomt dan verwarring.
Enkelvoudige stof
Een enkelvoudige stof, of niet-ontleedbare stof, is een zuivere stof die is opgebouwd uit slechts één chemisch element.
Zie ook
- Ontstaan van de verschillende elementen
- The Elements
Bronnen, noten en/of referenties
|
| Zie de categorie Chemisch element van Wikimedia Commons voor mediabestanden over dit onderwerp. |
Chemische elementen en isotopen | ||||||
|---|---|---|---|---|---|---|
|
Categorie:
- Chemisch element
(window.RLQ=window.RLQ||[]).push(function()mw.config.set("wgPageParseReport":"limitreport":"cputime":"0.096","walltime":"0.132","ppvisitednodes":"value":445,"limit":1000000,"ppgeneratednodes":"value":0,"limit":1500000,"postexpandincludesize":"value":8528,"limit":2097152,"templateargumentsize":"value":1606,"limit":2097152,"expansiondepth":"value":8,"limit":40,"expensivefunctioncount":"value":0,"limit":500,"unstrip-depth":"value":0,"limit":20,"unstrip-size":"value":398,"limit":5000000,"entityaccesscount":"value":1,"limit":400,"timingprofile":["100.00% 96.862 1 -total"," 38.11% 36.912 1 Sjabloon:Commonscat"," 16.55% 16.033 1 Sjabloon:Navigatie_elementen"," 14.17% 13.723 1 Sjabloon:Navigatie"," 12.11% 11.733 1 Sjabloon:Zie_hoofdartikel"," 10.65% 10.320 1 Sjabloon:Appendix"," 8.76% 8.484 1 Sjabloon:Navigatie/Tabel"," 7.94% 7.690 1 Sjabloon:Multiparameters"," 5.92% 5.735 1 Sjabloon:References"," 5.44% 5.268 1 Sjabloon:Woordenboek"],"scribunto":"limitreport-timeusage":"value":"0.003","limit":"10.000","limitreport-memusage":"value":523655,"limit":52428800,"cachereport":"origin":"mw1326","timestamp":"20190329014355","ttl":2592000,"transientcontent":false);mw.config.set("wgBackendResponseTime":116,"wgHostname":"mw1325"););